1. はじめに
創薬研究において、候補化合物のADMET特性(吸収・分布・代謝・排泄・毒性)を早期に評価することは、開発の成功率を高めるために欠かせません。しかし、単にADMETを予測するだけでなく、その結果を踏まえて化合物の構造を最適化できれば、創薬プロセスの効率はさらに向上します。こうした「予測」と「最適化」の両立を実現するのが「admetSAR 3.0」です。
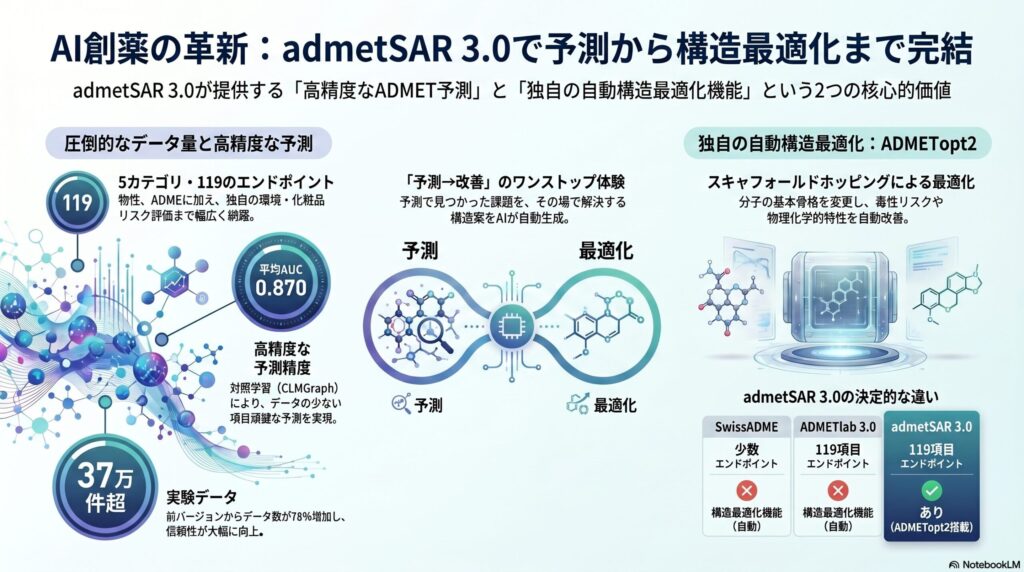
admetSAR 3.0は、華東理工大学(East China University of Science and Technology, ECUST)のTang Yunグループが開発し、2024年にNucleic Acids Research誌に発表された無料のADMET予測・最適化Webプラットフォームです。2012年の初版、2019年のv2.0を経て、v3.0では対照学習ベースのCLMGraphフレームワーク、119エンドポイントへの拡張、37万件超の実験データ、そしてスキャフォールドホッピングによる構造最適化モジュールADMETopt2など、大幅な進化を遂げました。
本記事では、admetSAR 3.0のCLMGraphフレームワーク、119エンドポイントの内訳、予測精度、構造最適化の仕組み、そしてADMETlab 3.0やSwissADMEとの比較までを詳しく解説します。この記事を読むことで、以下の内容が理解できます。
・admetSAR 3.0のCLMGraphフレームワークの仕組み(対照学習+マルチタスクGNN)
・5カテゴリ119エンドポイントの内訳と臨床的意義
・平均AUC 0.870、PCC 0.70超82%という予測精度の根拠
・ADMETopt2によるスキャフォールドホッピング型の構造最適化
・SwissADME・pkCSM・ADMETlab 3.0との精度比較と使い分け
・予測の信頼性を確保する多層的な検証アプローチ
AI創薬やADMET評価に関心のある研究者・薬剤師の方にとって、admetSAR 3.0を実践的に活用するためのガイドとなれば幸いです。
2. admetSAR 3.0とは?予測と最適化を両立するAI創薬プラットフォーム
admetSAR 3.0は、華東理工大学(ECUST)の薬学院・Tang Yunグループが開発・運営する、化合物のADMET特性予測・最適化を行う無料のWebプラットフォームです。2024年7月にNucleic Acids Research誌(Gu Y et al., 2024, NAR, Vol.52(W1):W432-W438)で詳細が報告されています。
admetSARは2012年の初版から12年以上にわたり開発が続けられており、v2.0(2019年)を経てv3.0(2024年)では大幅な機能拡張が行われました。v3.0の主な進化は、化合物数で9.01%(10万4,652種)、データレコードで78.08%(37万件超)、エンドポイント数で108.77%(119項目)の増加です。
さらにadmetSAR 3.0は、予測だけでなく「検索」「予測」「最適化」の3モジュールを統合的に提供する点が大きな特徴です。ADMETopt2モジュールにより、予測結果に基づいてクエリ分子の構造を自動的に最適化できます。
URL:https://lmmd.ecust.edu.cn/admetsar3/
3. CLMGraphフレームワーク:対照学習とマルチタスクGNNの融合
admetSAR 3.0の予測精度を支える中核技術が、CLMGraph(Contrastive Learning based Multi-Task Graph Neural Network)です。これは、対照学習(Contrastive Learning)による自己教師あり事前学習と、108のADMETタスクを同時学習するマルチタスク学習を組み合わせたグラフニューラルネットワーク(GNN)フレームワークです。
CLMGraphは3つの主要モジュールで構成されます。入力モジュールでは化合物を分子グラフ(ノード行列とエッジ特徴行列)に変換します。特徴抽出モジュールではGNNを用いてノードとエッジの情報を更新し、さらに対照学習により増強された分子グラフペア間の相互情報を最大化することで、ラベルデータが不足しているエンドポイントでも強力な分子表現を獲得します。ADMET予測モジュールでは、108のタスクを共同学習させ、関連するエンドポイント間で情報を共有・活用します。
この設計により、従来の単一タスク学習モデルよりも頑健で精度の高い予測が実現されています。特に、実験データが少ないエンドポイントでも事前学習の恩恵により予測精度が維持される点が、CLMGraphの大きな利点です。
4. 119のADMETエンドポイント:5カテゴリで包括的にカバー
admetSAR 3.0が予測する119のエンドポイントは、以下の5つのカテゴリに分類されています。
・基本物性(Basic Properties):logP、溶解度(logS)、分子量、TPSAなど
・ADME物性(ADME Properties):Caco-2透過性、肝代謝安定性、半減期、血漿タンパク結合率など
・ヒト健康毒性(Human Health Toxicity):Ames試験、発がん性、hERG阻害、肝毒性、生殖毒性など
・環境リスク評価(Environmental Risk):生分解性、生物濃縮性、魚毒性など
・化粧品リスク評価(Cosmetic Risk):皮膚刺激性、眼刺激性、感作性など
特に、環境リスクと化粧品リスクの評価機能は、他のADMET予測ツールにはあまり見られない独自の強みです。医薬品だけでなく、化粧品成分や環境化学物質の評価にも応用できる汎用性を備えています。
5. admetSAR 3.0の予測精度:AUC 0.870とPCC 0.70超の実力
admetSAR 3.0の予測精度は、5分割交差検証と外部検証セットによって厳密に評価されています。論文に報告されている主要な評価指標は以下の通りです。
・分類モデル(90エンドポイント)の平均AUC:0.870
・回帰モデル:82%以上のエンドポイントでPCC(ピアソン相関係数)0.70超
・代表的エンドポイントのAUC:Caco-2透過性 0.95、HIA 0.977、BBB 0.927、Ames変異原性 0.88
・代表的エンドポイントのPCC:logS(溶解度)0.961、logP(分配係数)0.968、Caco-2透過性 0.857
ただし、半減期や平均滞留時間など一部の複雑な薬物動態パラメータでは、予測性能がやや低下する場合があります。こうした限界を理解した上で予測結果を活用することが重要です。
6. ADMETopt2:スキャフォールドホッピングによる構造最適化
admetSAR 3.0の最大の差別化ポイントが、ADMETopt2という構造最適化モジュールです。ADMETopt2は、スキャフォールドホッピング(基本骨格の変更)と分子変換ルールを用いて、クエリ分子のADMET特性を自動的に最適化する機能を提供します。
例えば、予測の結果「BBB透過性が低すぎる」「hERG阻害リスクが高い」といった問題が見つかった場合、ADMETopt2はその問題を改善する方向に分子構造を変更した候補化合物を自動生成します。研究者は生成された候補の中から、元の生理活性を維持しつつADMETプロファイルが改善されたものを選定できます。
この「予測→問題特定→自動最適化」というワンストップのワークフローは、他のADMET予測ツールにはない独自の価値を提供します。
7. admetSAR 3.0と他のADMET予測ツールの比較
admetSAR 3.0は他の主要ADMETツールと比べて以下の位置づけにあります。
・SwissADME:BOILED-Eggモデルによる視覚化が強み。予測精度ではadmetSAR 3.0やADMETlab 3.0に劣る場面も。
・pkCSM:28エンドポイント、グラフベースシグネチャによる独自アプローチ。admetSAR 3.0は網羅性・最適化機能で優位。
・ADMETlab 3.0:119エンドポイント、Multi-task DMPNNで高精度。網羅性は同等だが、admetSAR 3.0はADMETopt2による構造最適化機能で差別化。
・ADMET-AI:大規模ライブラリの一括評価に特化。admetSAR 3.0は環境・化粧品リスク評価で独自の強み。
実務的には、予測の網羅性と精度を求めるならADMETlab 3.0とadmetSAR 3.0を併用し、構造最適化まで踏み込むならadmetSAR 3.0のADMETopt2を活用するのが効果的です。SwissADMEで初期スクリーニング→詳細予測をadmetSAR 3.0またはADMETlab 3.0で実施→最適化をadmetSAR 3.0で行う、という段階的アプローチが理想的です。
8. まとめ:admetSAR 3.0が創薬ADMET評価にもたらす価値
本記事では、admetSAR 3.0について、CLMGraphフレームワーク、119エンドポイントの内訳、予測精度、構造最適化モジュール、そして他ツールとの比較を解説しました。
admetSAR 3.0がAI創薬研究者にとって価値ある理由は、第一に対照学習とマルチタスクGNNを融合したCLMGraphによる高精度予測(平均AUC 0.870)、第二に5カテゴリ119エンドポイントの包括的カバレッジと環境・化粧品リスク評価の独自性、第三にADMETopt2によるスキャフォールドホッピング型の構造最適化機能です。予測から最適化までをワンストップで提供する点は、他のADMET予測ツールにはない大きな差別化要素です。
ただし、予測結果はあくまで計算値であり、信頼性を確保するには複数ツールでの比較、アプリケーションドメインの確認、そして最終的な実験的検証が不可欠です。admetSAR 3.0を研究ワークフローに組み込み、ADMETlab 3.0やSwissADMEと併用しながら、より信頼性の高い創薬判断を実現してみてください。
参考文献
・Gu Y, Yu Z, Wang Y, Chen L, Lou C, Yang C, Li W, Liu G, Tang Y. admetSAR3.0: a comprehensive platform for exploration, prediction and optimization of chemical ADMET properties. Nucleic Acids Research, 2024, 52(W1):W432-W438:https://academic.oup.com/nar/article/52/W1/W432/7655777
・admetSAR 3.0公式サイト:https://lmmd.ecust.edu.cn/admetsar3/
・admetSAR論文(初版, 2012):https://pubs.acs.org/doi/abs/10.1021/ci300367a
免責事項
本記事は、AI創薬におけるADMET予測プラットフォームに関する情報提供を目的として作成されたものです。記事の内容は、公開時点で入手可能な文献・情報に基づいていますが、技術の進歩や新たな知見により、情報が変更される場合があります。記事に記載されたソフトウェアの使用結果や、それに基づく研究成果について、筆者および本ブログは一切の責任を負わないものとします。実際の創薬研究や臨床応用にあたっては、必ず最新の文献・公式ドキュメントを確認し、専門家の助言を得てください。
本記事は生成AIを活用して作成しています。内容については十分に精査しておりますが、誤りが含まれる可能性があります。お気づきの点がございましたら、コメントにてご指摘いただけますと幸いです。
Amazonでこの関連書籍「図解 生物薬剤学・薬物動態学 (みてわかる薬学)」を見る